北虫草液体培养基配方的优化
邹湘月1,2罗巍1,2吴郑武1,2刘东波1,2谢红旗1,3*
(1 湖南农业大学园艺园林学院,湖南长沙 410128;2 国家中医药管理局亚健康干预技术实验室,湖南长沙 410128;3 湖南省作物种质创新与资源利用重点实验室,湖南长沙 410128)
《食用菌》2.12.4
摘要 以发酵液中北虫草生物量、胞内胞外多糖含量为指标,筛选出最佳碳源为玉米粉,最佳氮源为麸皮,KH2PO4和ZnSO4为最适无机盐。通过三因素三水平的正交实验,优化出北虫草菌丝生物量及多糖得率的液体发酵培养基,最佳配方为玉米粉4.8%,麸皮0.6%,KH2PO40.05%,ZnSO4·7H2O0.1%。
关键词 北冬虫夏草 培养基 多糖得率 优化
北虫草(Cordyceps militaris L.Link),又称北冬虫夏草,俗称蛹虫草,是冬虫夏草种的一种[1]。
近年来,人们在北冬虫夏草适宜生长条件的选择及控制、液体菌种代替固体菌种等种植技术方面取得了系列成就,特别是液体发酵技术的深入研究,能够快速地生产药食用菌的真菌菌丝体,降低杂菌感染,提高有效成分含量,大大缩短了传统固体培养时间,有效节约生产成本[5],[6]。目前,对北冬虫夏草液体菌种的适宜碳源、氮源及其配方的报道较多[7]-[9],但是充分考虑培养基成分对菌种生物量、细胞内外多糖含量影响的系统性研究却甚少。研究通过系列对比试验,探讨不同碳源、氮源及其无机化合物对上述3种指标的影响,为生产实践中的液体菌种制备研究出可靠的相关技术参数;通过正交实验,优化出有利于菌丝胞内外多糖累积的最佳培养基配方,为北虫草的液体发酵生产提供借鉴参考。
1 材料与方法
1.1 供试材料
1.1.1 供试菌种 由湖南农业大学食用菌研究所提供。
1.1.2 试剂和器材 葡萄糖、蔗糖、KH2PO4、MgSO·7H2O、FeSO4·7H2O、CaCl2·H2O、MnSO4·H2O、ZnSO4和NH4NO3均为分析纯试剂;酵母膏和蛋白胨均为生化试剂;玉米粉、麸皮和豆饼粉均为煮沸30min后四层纱布滤过液。
立式压力蒸汽灭菌器(LDZX-50FAS),上海申安医疗器械厂;超净工作台(SW-CJ-2F型),苏州净化设备有限公司;恒温培养振荡器(ZHWY-2102C型),上海制成分析仪器制造有限公司;电热鼓风干燥箱(101-4AB型),北京中兴伟业仪器有限公司;恒温水浴锅(DK-S24),上海精宏实验设备有限公司;台式离心机(KA-1000型),上海安亭科学仪器厂;紫外分光光度计(U-1800型)日本岛津公司;其他为实验室常规设备。
1.1.3 培养基 固体培养基(PDA):马铃薯汁200g/L,葡萄糖20g/L,酵母膏1.0g/L,蛋白胨2.0g/L,KH2PO41.0g/L,MgSO40.5g/L,VBl0.02g/L,琼脂20g/L,pH6.7,121℃0.1MPa蒸汽灭菌30min,用于菌种活化培养。
种子液体培养基:KH2PO43.0g/L,MgSO41.5g/L,蛋白胨10g/L,葡萄糖20g/L,pH6.7,高压蒸汽灭菌30min。
基本发酵液体培养基:KH2PO41.0g/L,MgSO4·7H2O0.05g/L,氮源6.0g/L,碳源36g/L,pH6.7,在121℃0.1MPa高压蒸汽下灭菌30min。
1.2 培养方法
1.2.1 各培养基培养方法 固体培养:将保存的菌种接种于固体培养基,置于24℃恒温培养7~10d[10],备用。种子液培养:将活化的菌种接种于种子培养基中,25℃、120r/min于恒温培养振荡器中黑暗培养7~8d至菌种成熟[11]。发酵培养:按4%(体积分数)的接种量将培养好的液体种子接种到发酵培养基中,24℃、120r/min,恒温振荡黑暗培养8~10d[12]。
1.2.2 液体发酵培养基的筛选试验
1.2.2.1 碳源的确定 在基本发酵液体培养基中。碳源分别用葡萄糖、蔗糖、可溶性淀粉、玉米粉、麸皮代替,质量分数为3.6%,pH6.7。每组设3个重复,液体发酵培养。
1.2.2.2 氮源的确定 在基本发酵液体培养基中.氮源分别用蛋白胨、酵母膏、麸皮、豆饼粉、硝酸铵代替,质量分数为0.6%,pH6.7。每组设3个重复,液体发酵培养。
1.2.2.3 无机化合物的确定 在基本培养基中分别加入KH2PO4、MgSO4·7H2O、FeSO4·7H2O、ZnSO4·7H2O、MnSO4·H2O、CaCl2·H2O每种无机化合物的添加量为质量分数0.1%,pH6.7。每组设3个重复,液体发酵培养。
1.3 测定方法
1.3.1 菌丝体生物量的测定 将发酵液抽滤得到菌丝体滤饼,收集上清液和沉淀的菌丝体,用蒸馏水洗后,再离心,直至上清液不再带有培养基的颜色为止。收集菌丝体,置于60℃干燥箱中干燥至恒重,在干燥器中冷却到常温,称重。
1.3.2 虫草胞外多糖提取 北虫草液体摇瓶发酵液经4层纱布过滤,将得到的滤液进一步用滤纸过滤,取滤液10mL,加4倍体积的95%乙醇,于4℃下醇沉24h,在转速为3000r/min条件下离心15min,沉淀多糖用蒸馏水复溶后于4℃下保存。
1.3.3 虫草胞内多糖提取 准确称取干燥的虫草菌丝体1.00g,加蒸馏水30mL,于90℃提取2h,趁热过滤,滤渣加蒸馏水30mL,于90℃水浴浸提2h,合并滤液,定容至100mL.取溶液10mL,加4倍体积95%乙醇,于4℃下醇沉24h,离心,沉淀加适量蒸馏水于4℃下保存。
1.3.4 多糖的测定 多糖采用苯酚-浓硫酸法测定[13]。
1.4 正交实验 依据北虫草发酵生长需要的营养需求和实验的可行性,按照1.2.2筛选出的培养基的各个成分,采用L9(33)正交表,对发酵培养基进行三因素三水平的正交实验。优化出液体发酵培养基的最佳搭配方案。表1为正交实验的因素与水平的选择。
表1 正交实验L 9 (3 3 )因素和水平
水平 碳源/% 氮源/% 无机盐/%
1 2.4 0.6 KH2PO40.05%+ZnSO4·7H20 0.05%
2 3.6 1.2 KH2PO40.05%+ZnSO4·7H20 0.1%
3 4.8 1.8 KH2PO40.05%+ZnSO4·7H20 0.15%
2 结果与分析
2.1 碳源的选择
2.1.1 碳源对北虫草菌丝体生物量的影响 碳源是北虫草合成碳水化合物及氨基酸的基础,实验结果表明(图1所示),5种不同碳源都能被北虫草不同程度利用,以蔗糖做碳源时,菌丝体干重达最大值25.6g/L,葡萄糖、玉米粉次之,其次为可溶性淀粉,麸皮最差,约为蔗糖碳源的30%。这一结果进一步证明了北虫草菌丝体的液体发酵对蔗糖等小分子糖类的利用率较高。
2.1.2 碳源对北虫草菌丝体胞外多糖和胞内多糖得率的影响 多糖是菌丝体细胞壁的主要成分之一,当碳源不适时合成速率降低从而导致多糖得率的下降。图2可见从多糖方面考虑,以麸皮作为碳源的胞外多糖含量较高,为3.0764mg/mL,玉米粉次之;以玉米粉作为碳源时的胞内多糖含量较高,达到50.79mg/g,约为葡萄糖、可溶性淀粉、蔗糖碳源的4至5倍。综合考虑生物量及多糖含量影响因素,采用玉米粉作为北虫草液体发酵的碳源。该结果与王永敏[14]等人得出的蔗糖为蛹虫草发酵条件的最适碳源有所区别,这可能是因为北冬虫夏草的菌种不同所致。
2.2 氮源的选择
2.2.1 氮源对北虫草菌丝体生物量的影响 氮源是北虫草自身合成蛋白质及核酸的必需元素,菌丝体对氮源的利用有很大的选择性[14]。由图3可知,以有机氮作为北冬虫夏草液体发酵的氮源,其生物量优于无机氮源,各有机氮源之间的差别并不显著。其中,蛋白胨作为氮源时,生物量最高,达到19.9g/L,约为以硝酸铵作氮源时的2倍。加入硝酸铵的液体培养基中生物量最低,可能是因为酸性盐的使用导致发酵液pH降低得过快,不能为北虫草提供适宜的发酵环境从而抑制了菌丝体的生长[7]。
2.2.2 氮源对北虫草菌丝体胞外多糖和胞内多糖得率的影响 由图4可知,从多糖方面考虑,酵母浸膏作为氮源,其菌丝体中的胞外多糖含量可达1.426mg/mL;以麸皮作为氮源,菌丝体中胞内多糖含量为38.6mg/g;较差的是硝酸铵。从氮源的影响因素来看,麸皮对胞内和胞外多糖的合成有明显的促进作用。综合考虑上述影响及经济原则,选用麸皮为北虫草发酵的最佳氮源。
2.3 无机化合物的选择
2.3.1 无机盐对北虫草菌丝体生物量的影响 试验结果表明(图5),各种无机盐都对北冬虫夏草菌丝体生物量有促进作用,说明这些无机成分是北冬虫夏草菌丝生长的必不可少的成分。其影响效果依次是:1.ZnSO4;2.KH2PO4;3.FeSO4;4.CaCl2;5.MnSO4;6.MgSO4。其中Zn2+对北冬虫夏草菌丝体生长影响较大,生物量可达14.5g/L,从北冬虫夏草菌丝体生物量考虑,选择KH2PO4和ZnSO4作为北冬虫夏草菌丝体液体发酵的无机盐。
2.3.2 无机盐对北虫草菌丝体胞外多糖和胞内多糖得率的影响 如图6所示,添加Zn 2+有利于北冬虫夏草发酵液和菌丝体内多糖的积累,其含量分别是0.65mg/mL,32.9mg/g;对北冬虫草菌丝体胞内胞外多糖含量影响排序依次是:硫酸锌>硫酸亚铁>磷酸二氢钾>硫酸镁>氯化钙>硫酸锰。从北冬虫夏草菌丝体胞外和胞内多糖含量考虑,选择KH2PO4和ZnSO4作为北冬虫夏草菌丝体液体发酵的无机盐。
2.4 正交实验结果 分别以提高北虫草发酵液中多糖和菌丝体内多糖含量为实验目的,对培养基成分进行的三因素三水平的正交实验,结果见表2。由直观分析表(表3)可知,三因素对胞外和胞内多糖含量的影响大小次序相同,都是碳源>氮源>无机盐。极差R最大的是A因素(胞外:1.7;胞内:28.8),其次为B因素(胞外0.9;胞内15.2),最后是C因素(胞外0.4;胞内6.6)。极差越大说明该因素的变动对结果的影响越大,即碳源是最重要的影响因素。由方差分析结果(表4)可知,两指标实验的A因素都达到差异极显著(P<0.01),B因素都达到差异显著(0.01<P<0.05),而C因素差异不显著(P>0.05),此结论与直观分析表所得结果基本一致并说明了A和B因素应选取最优水平,因素C选取任一水平对实验结果影响不明显。因此从表2和表3结果得出,KA中K3最大,KB中K1为最大值,KC中K2最大,所以A因素选水平3,B因素选水平1,理论上C因素可选任一水平。在本正交实验计划表中A3B1C2(玉米粉4.8%,麸皮0.6%,KH2PO40.05%,ZnSO4.7H2O0.1%)为最优方案,其菌丝体胞外和胞内多糖含量分别达到了3.1mg/mL和50.1mg/g。
表2 胞外多糖正交试验直观分析表
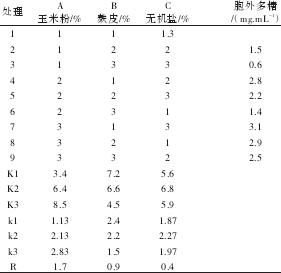
表3 胞内多糖正交试验直观分析

表4 胞外多糖正交实验方差分析表
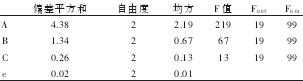
表5 胞内多糖正交实验方差分析表
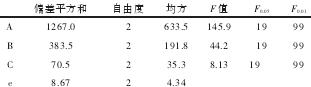
3 结论与讨论
对碳氮源的筛选结果表明,北冬虫夏草可利用的碳氮源比较广泛,对碳源来说,北虫草对双糖、单糖、有机碳源有较好利用。对于氮源来说,北虫夏草对有机氮源和天然氮源的利用较好。适量的无机盐可以促进北冬虫夏草菌丝体的生长和胞外胞内多糖的积累,并得出适合北冬虫草液体发酵的最优培养基搭配方案为玉米粉4.8%,麸皮0.6%,KH2PO40.05%,ZnSO4·7H2O0.1%。另外,胞内外多糖含量不随生物量的增加而增加,且两者间相关性不明显。但是,研究仅对培养基进行了优化,要使北虫草多糖的含量进一步提高,还必须对培养条件,包括培养温度、时间、转速、装液量、起始pH,接种量等因素进行优化,还有待于进一步研究。
参考文献
[1]许超德.冬虫夏草的研究进展[J].菌物研究,2006,4(2):60-64.
[2]张平,朱述钧,钱大顺,等.北冬虫夏草功能成分及保健作用分析[J].江苏农业科学,2003(6):105-107.
[3]孟兆丽,朱凯,冯云,等.蛹虫草多糖抑菌及抗氧化作用研究[J].食品研究与开发,2008,29(9):31-33.
[4]徐雷雷,王静风.蛹虫草降血糖作用及其机制研究[J].中国药理学通报,2011,27(9):1331-1332.
[5]王建芳,杨春清.蛹虫草人工栽培及产品开发研究概况[J].时珍国医国药,2006(2):268.
[6]章克昌.药用真菌研究开发的现状及其发展[J].食品与生物技术学报,2002,21(1):99-103.
[7]方华舟,贾瑞,程利霞,等.不同培养基原料及配方对北冬虫夏草液体菌种质量的影响[J].贵州农业科学,2011,39(2):105-109.
[8]傅岚,黄红英.古尼虫草液体深层发酵条件的研究[J].湖南师范大学自然科学学报,2004,27(2):71-74.
[9]杨荣玲,陈卫东.巴西虫草液体培养条件的优化[J].中国食用菌,2007,26(1):50-54.
[10]祝长杰,李小宇.蛹虫草001号高产菌株栽培实验[J].湖南农业科学,2010(9):41-42.
[11]龚兰芳.玉溪市蛹虫草栽培技术[J].中国林副特产,2008(6):35-37.
[12]罗巍,刘东波.蛹虫草液态发酵过程中有效成分的动态积累变化[J].食品与发酵工业,2011,37(9):108-111.
[13]来永彬,王琦.蛹虫草多糖含量的测定与分析[J].中成药,2001,23(7):517-518.
[14]王永敏,祝文兴.优化条件对蛹虫草菌丝体与胞外多糖得率研究[J].济南大学学报,2010,24(2):148-151.

